Изотермический процесс
Изотермический процесс — это изопроцесс, происходящий при постоянной температуре: Τ = const.
Закон экспериментально открыли независимо друг от друга английский химик и физик Роберт Бойль (1662) и французский физик Эдм Мариотт (1676).
Закон изотермического процесса (Бойля-Мариотта): для данной массы газа при постоянной температуре произведение давления на объем есть величина постоянная: T = const или для двух состояний pV=const
Для осуществления изотермического процесса надо сосуд, наполненный газом, привести в контакт с термостатом.
Термостат — это прибор для поддержания постоянной температуры. Подробнее см. wikipedia
Изотермическим процессом приближенно можно считать процесс медленного сжатия или расширения газа в сосуде с поршнем.
Термостатом в этом случае служит окружающая среда.
Изобарный процесс
Изобарный процесс — это изопроцесс, происходящий при постоянном давлении: p = const.
baros — тяжесть, вес.
Закон экспериментально исследовали независимо друг от друга французские физики Жак Шарль (1787) и Жозеф Гей-Люссак (1802).
Работа Ж. Шарля была опубликована уже после открытия Ж. Гей-Люссака. Но изобарный процесс в российских учебниках называют законом Гей-Люссака, в белорусских — законом Шарля.
Закон изобарного процесса: при данной массе газа при постоянном давлении отношение объема к абсолютной температуре есть величина постоянная: p = const или 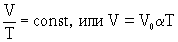
Опыт показывает, что при малых плотностях температурный коэффициент объемного расширения не зависит от вида газа, т.е. одинаков для всех газов).
Получить изобарный процесс можно при помощи цилиндра с невесомым поршнем.
Изохорный процесс
Изохорный процесс — это изопроцесс, происходящий при постоянном объеме: V = const.
chora — занимаемое место, объем.
Закон экспериментально исследовали независимо друг от друга французские физики Жак Шарль (1787) и Жозеф Гей-Люссак (1802).
Изохорный процесс в российских учебниках называют законом Шарля, в белорусских — законом Гей-Люссака.
Закон изохорного процесса: при данной массе газа при постоянном объеме отношение давления к абсолютной температуре есть величина постоянная:
V = const или 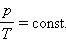
Получить изохорный процесс можно в баллоне, который не изменяет свой объем при данном изменении температуры.
Тщательная экспериментальная проверка современными методами показала, что уравнение состояния идеального газа и вытекающие из него законы Бойля-Мариотта, Гей-Люссака и Шарля достаточно точно описывают поведение реальных газов при небольших давлениях и не слишком низких температурах.
